作者简介:闫艳华(1985—),女,山西吕梁人,硕士,从事植物遗传与分子生物学方面的工作,E-mail: yanhua19852008@163.com。
以5个不同品种的燕麦种子和叶片为原料,用CTAB法提取燕麦基因组DNA,最后通过吸光度来检测所提取DNA的纯度和质量,确保提取出纯度较高的燕麦基因组DNA样品。结果表明,燕麦叶子基因组DNA比燕麦种子基因组DNA要容易提取得多,得到的DNA溶液质量比较高,而这5种燕麦的基因组DNA的提取难易程度不同,只有符合要求纯度的燕麦基因组DNA才可以用于进一步研究。
燕麦属于禾本科燕麦属一年生草本植物, 分为有壳和无壳两大类, 即皮燕麦和裸燕麦。燕麦抗旱、抗寒, 是我国主要高寒作物之一, 在贫苦地区是不可缺少的干粮, 市场开发前景广阔[1, 2, 3, 4, 5]。但是燕麦DNA提取过程中易受纤维、蛋白质、酚类, 脂类、糖类及其他干扰物质含量的影响, DNA提取的质量较差, 严重影响燕麦分子生物学方面的研究与进展[6, 7, 8]。
本研究旨在用燕麦叶片和种子两种不同材料通过改良的CTAB法得到优质的基因组DNA, 为进一步研究奠定基础。
供试燕麦种子由吕梁学院生物实验室提供, 保存于4 ℃冰箱内。5个品种分别是定燕1号、白燕2号、宁莜1号、晋燕17号和晋燕8号。
主要试剂有无水乙醇、氯仿、异戊醇、CTAB(十六烷基三甲基溴化铵)、Tris(三羟甲基氨基甲烷)、EDTA(乙二胺四乙酸)、氯化钠、2-巯基乙醇、浓盐酸、氢氧化钠、蒸馏水等。
主要仪器有HH-6型数显恒温水浴锅、Neofuge13R型台式高速冷冻离心机、UV-1601双光束紫外/可见分光光度计、超低温冰箱、pH值试纸、玻璃棒、移液器、研钵、1.5 mL的离心管、电子天平、微波炉。
1.2.1 提取DNA的方法与步骤
采取CTAB法对燕麦基因组DNA进行提取。植物材料经过粉碎, 提取液中的阳离子去垢剂十六烷基三甲基溴化铵(CTAB)能够溶解细胞膜和核膜, 解聚核蛋白, 且与DNA形成复合物。在高盐条件下, 该复合物是可溶的[9]。用氯仿等有机溶剂抽提可使蛋白质变性, 使多糖沉淀, 经过离心, CTAB-DNA复合物仍留在上清液中; 降低盐浓度, 则CTAB-DNA复合物发生沉淀, 沉淀用高盐TE缓冲液溶解后, 加入无水乙醇, CTAB仍留在溶液中, 但DNA发生沉淀, 沉淀溶于TE缓冲液中, 即可得到植物基因组DNA[9]。
1.2.2 备用试剂的配制
氯仿/异戊醇。按照体积比24∶ 1的比例配制即可, 在4 ℃下保存备用。
CTAB/NaCl溶液。4.1 g NaCl溶解于80 mL蒸馏水中, 缓缓加入10 g CTAB, 边加热边搅拌至溶解, 用蒸馏水定容至100 mL。
TE缓冲液。10 mL 0.01 mol· L-1pH值8.0的Tris-HCl和40 mL 0.001 mol· L-1 pH值8.0的EDTA混合, 加入蒸馏水定容至100 mL, 配制成TE缓冲液。
pH值8.0 Tris-HCl。50 mL 0.2 mol· L-1的Tris加26.8 mL的0.2 mol· L-1的HCl, 定容至200 mL。
pH值8.0 CTAB提取液。2 g CTAB加蒸馏水40 mL, 加0.1 mol· L-1Tris-HCl(pH值8.0)10 mL、0.5 mol· L-1EDTA(pH值8.0)4 mL和5 mol· L-1NaCl 28 mL, 待CTAB溶解后用蒸馏水定容到100 mL。
1.2.3 DNA的提取
燕麦种子在清水中浸泡后除去外壳, 放在预冷的研钵内迅速磨碎, 用电子天平称取0.1 g燕麦种子粉末, 转入1.5 mL无菌离心管。
将一定量CTAB提取液中加入2-硫基乙醇至终体积分数的2%, 在水浴锅中加温至65 ℃。然后向上述装有燕麦种子粉末的离心管中加入600 μ L的预热CTAB提取液, 在65 ℃的水浴锅中保温30 min, 期间不断摇晃离心管。
向上述离心管中加入500 μ L的氯仿/异戊醇, 颠倒离心管数次, 然后在4 ℃, 11 000 r· min-1下离心10 min, 取上清液转移到另一个离心管中。
向上清液中加入1/10体积的CTAB/NaCl溶液并预热到65 ℃, 颠倒离心管数次。再向离心管中加入相同体积的氯仿/异戊醇, 晃动离心管几次。室温, 11 000 r· min-1下离心10 min, 用移液管吸取上清液转移到另一个离心管中。
然后再加入等体积的氯仿/异戊醇, 相同条件下重复离心几次, 直到中间没有白色物质, 取上清到一个无菌离心管中。
向上述离心管中加入2倍体积的无水乙醇, -20 ℃下静置30 min。
在4 ℃条件下, 14 000 r· min-1离心15 min, 弃上清, 留下沉淀物。
沉淀用75%的乙醇润洗1次, 室温干燥, 用TE缓冲液溶解沉淀, 得到DNA溶液, 在-20 ℃下保存备用。
叶片DNA的提取方法和步骤与种子基本一样。
核酸之所以具有紫外吸收的性质, 是因为其碱基均具有共轭双键。核酸在260~290 nm处有较强吸收峰, 在260 nm处吸收值最大, 230 nm吸收值最小; 蛋白质在280 nm处吸收值最大。因此可以根据所测定样品的D260/D280的比值来判断提取的DNA的纯度。
在紫外分光光度计上分别设置260、280 nm两个波长, 用TE缓冲液进行空白对照, 对每种燕麦提取的基因组DNA溶液进行吸光度测定, 并计算D260/D280。
D值检测燕麦中提取的基因组DNA纯度的标准是由D260, D280和D260/D280的比值来判断的, 当D260/D280≈ 1.8时, DNA纯度最高; 当D260/D280< 1.8时, 说明有蛋白质等杂质; 当D260/D280≈ 2.0时, 说明RNA含量较高, DNA降解多[10]。
由表1可知, 宁莜1号种子的D260/D280> 2.00, 而且在260 nm时吸光度最大, 说明宁莜1号在DNA提取过程中有RNA的干扰。晋燕17号种子中提取的DNA在280 nm下D值较大, 说明在提取过程中没有很好的抽提掉蛋白质, 排除蛋白质的干扰。由吸光度比值可知, 定燕1号提取的DNA纯度最高, 其次是白燕2号、晋燕17号和晋燕8号, 最后是宁莜1号。燕麦叶子中提取的DNA的D值基本与之保持一致。
| 表1 提取的5种燕麦基因组DNA吸光度 |
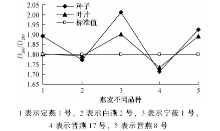
由图1可以看出, 叶片中DNA纯度次序基本与种子中一样, 叶片中提取的DNA的D260/D280趋向于1.80这条标准线。也就是说, 叶片中提取的DNA的质量和纯度比种子中提取的DNA的质量和纯度要高。总体上叶片中提取的DNA更加适合做燕麦基因组DNA模板, 用于下一步的研究。由此可知, 叶片比种子中的DNA更易提取, 或者说叶子中本身的干扰因素少。
燕麦的种子中含有较多的多糖、蛋白质和脂质, 这些物质都对燕麦基因组DNA的提取造成一定程度的干扰, 去除这些杂质是提取纯度较高的DNA的重要一步。叶子中虽含有多酚类物质较多, 但相对种子来说比较好抽提, 所以叶子中提取的DNA质量比种子中提取的DNA质量高。
本试验采用的是CTAB法提取燕麦2个部位的DNA。1)由检测结果看, CTAB法可得到较高质量总DNA, 从成本上看, 是较理想的方法[11]。2)氯仿/异戊醇抽提杂质时, 并不是一次就可以成功, 必须进行多次离心、多次抽提才可以把杂质最大程度的去除, 但有时会起到负作用。3)用无水乙醇沉淀DNA时, 乙醇的温度特别重要, 只有在低温下才可以较多的沉淀出DNA, 然后再在低温下进行离心才可以得到较多DNA沉淀; 如果温度没有控制好, DNA沉淀的会很少, 甚至已经沉淀的DNA裂解了, 以至于得不到高质量的DNA。4)EDTA在碱性溶液中才能较好的溶解, 在溶解EDTA时可以加入氢氧化钠。而CTAB必须在65 ℃左右才是液体状, 浓度高的CTAB低温下会变成胶状, 浓度低的CTAB在低温下会结晶。5)酚是芳香烃环上的氢被羟基取代的一类芳香族化合物。最简单的酚为苯酚。酚类化合物是指芳香烃中苯环上的氢原子被羟基取代所生成的化合物, 根据其分子所含的羟基数目可分为一元酚和多元酚。因为燕麦中多酚物质的影响, DNA很快会发生褐变, 2-巯基乙醇的存在有效防止了DNA的氧化褐变。6)本试验采取的CTAB法提取燕麦基因组DNA并没有适合所有的燕麦种类, 有些燕麦可能适合另外一些提取DNA的方法。但要想满足后续的分子生物学实验, 要求所提取的DNA必须纯度很高, 所以之后要根据提取的材料去找到一种最适合的方法, 确保提取到纯度、浓度都很大的DNA模板。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|