细胞最佳生长所需要的铁离子(Fe3+)浓度至少为1 mmol·L-1[4],虽然铁元素在地壳中的含量为第4位,但在自然环境中,Fe2+易被氧化成Fe3+,所以在自然的pH下铁元素多以氧化铁和氢氧化铁这2种不可溶的、非常稳定的多聚体形式(10~18 μm)存在于环境中,难以被生物利用[4,6-7]。但生物体通过不断的进化,利用各种机制在低铁的环境中去获取Fe3+,其中分泌嗜铁素(siderophores)获取Fe3+的途径最为常见[6,8]。这种特殊的铁螯合剂通过对难溶性铁的活化、吸收和运输来提供微生物本身对铁营养的需求[9]。随着不同嗜铁素的发现,人们对其研究兴趣日益加强,细菌、真菌、植物和藻类在缺铁的条件下均能产生嗜铁素。目前,大约有500多种嗜铁素已经被定性分析,其中研究比较多的是微生物产生的嗜铁素。而且各种类型的嗜铁素有非常大的差异,一般可以分成三大类,其功能既是一种生长或萌发的促进因子,也是一种毒力因子[10]。目前,国内学者报道了嗜铁素对植物种子萌发有促进作用[11,12,13]。
本文对从土壤中分离的假单胞菌菌株HZ-2的具体分类地位和其产生嗜铁素能力进行了系统全面的研究,为以后开发和应用嗜铁素类微生物代谢奠定基础,而菌株HZ-2所产生的嗜铁素有望成为一种新型的微生物农药制剂。
1 材料与方法
1.1 菌株
实验用的菌株假单胞菌菌株HZ-2是一株土壤根围植物有益细菌,从浙江杭州的番茄根际分离所得,分离、培养和纯化使用金氏培养基。保存在营养肉汤培养基(NB)(5 g牛肉提取物,10 g蛋白胨,5 g NaCl,20 g大米,1 000 mL H2O,pH 7.0~7.2)中,储存在-80 ℃冰箱中备用。
1.2 培养基
1.3 菌株HZ-2的鉴定
1.3.1 菌落培养性状与菌体形态特征观察
1.3.2 菌株生理生化指标的测定
1.3.3 菌株HZ-2的脂肪酸分析
参照MIDI公司的操作手册,将菌株HZ-2在NA培养基上活化,接种于Luria-Bertani琼脂培养基上37 ℃恒温培养24 h后取菌,经过甲基化等处理后提取脂肪酸进行气相色谱分析,最后使用美国MIDI公司开发的专业全自动微生物鉴定软件对菌株HZ-2进行脂肪酸组成分析。鉴定结果要结合菌株的培养特征、最高相似度SI(similarity index)的菌种名称等因素来决定最后的菌株命名。
1.3.4 菌株HZ-2的16S rDNA序列分析
1.4 菌株HZ-2所产嗜铁素的检测
1.4.1 通用CAS平板检测
CAS检测液的制备。将6 mL 10 mmol·L-1十六烷基三甲基溴化铵(HDTMA)置于100 mL容量瓶中,并用双蒸水适当稀释,将1.5 mL 1 mmol·L-1 FeCl3·6H2O和7.5 mL 2 mmol·L-1 CAS溶液混合,沿玻璃棒慢慢加入容量瓶中。将4.3 g无水哌嗪溶于水中并加入6.25 mL 12 mol·L-1盐酸,获得pH 5.6的缓冲液,然后将此溶液转入前述的容量瓶中,并用双蒸水定容至100 mL,121 ℃ 15 min灭菌后备用[21]。
CAS检测平板的制备。将配制好的1 mol·L-1 CaCl2溶液、1 mmol·L-1 MgSO4·6H2O溶液、10%的酸水解酪蛋白溶液121 ℃ 15 min单独灭菌后备用。分别取0.2 mL的CaCl2溶液、0.2 mL的MgSO4·7H2O溶液、6 mL 10%的酸水解酪蛋白溶液,加入生物缓冲溶液Pipes,调pH值至6.8~7.0。去离子水定容至100 mL,加入2 g琼脂粉,121 ℃ 15 min灭菌后,温度降至60 ℃时,加入5 mL已经配置好的CAS蓝色检测液,混合均匀。注意不要产生气泡,影响平板检测实验。然后按照每皿25 mL倾注于培养皿中。阳性反应通过CAS颜色从蓝色变为黄色或橙色来记录。记录CAS琼脂平板在菌落周围形成晕圈。
1.4.2 嗜铁素的定量检测
无铁培养基采用琥珀酸培养液,富铁培养基在无铁培养基中加入FeSO4·7H2O至浓度为100 μmol·L-1(可抑制嗜铁素的产生)。2种培养基分装到150 mL的三角瓶中,每瓶50 mL,121 ℃ 15 min灭菌后备用。实验中使用的所有玻璃容器都需要浸泡在6 mol·L-1 HCl中过夜,并多次用蒸馏水冲洗,以除去残留铁的痕迹[22]。
嗜铁素发酵液的制备。菌株HZ-2的菌体在营养肉汤培养基(NB)活化后,从NB平板菌种刮取一环菌体接种于上述装有50 mL 2种培养基的150 mL三角瓶中,180 r·min-1 28 ℃振荡培养24 h,再以10%(V/V)的接种量接种到装有50 mL培养基的体积为300 mL的三角瓶中,200 r·min-1 28 ℃振荡培养24 h,以获得最大产量的嗜铁素。发酵液于4 ℃ 10 000 r·min-1离心15 min,即获嗜铁素发酵上清液及其对照(无嗜铁素),用于后续嗜铁素定量测定。
取上述已经制备好的嗜铁素发酵上清液与等体积CAS检测液,反应达到平衡后,测定630 nm波长处的吸光度值(A),同法测定对照液的吸光度值(Ar),用A/Ar值来定量菌株HZ-2分泌嗜铁素的能力。
2 结果与分析
2.1 菌株HZ-2的菌落形态与菌体特征
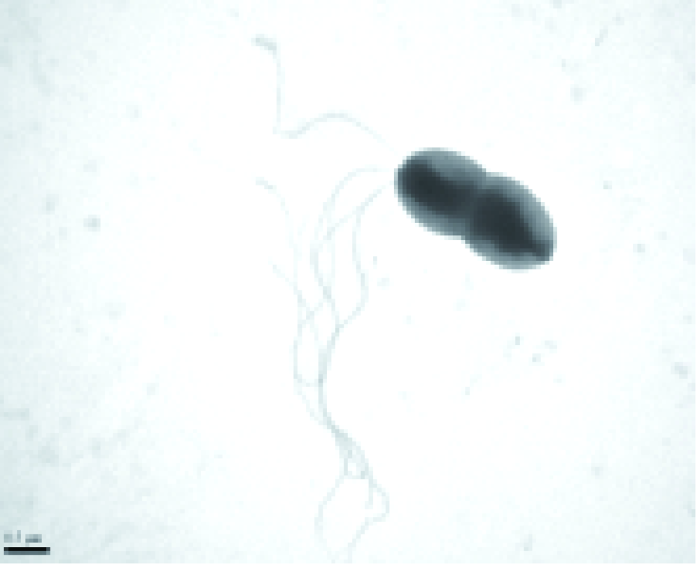
菌株HZ-2在NA平板培养基上培养48 h后观察到菌落呈扁平圆形,边缘齐整,略呈黄色,菌落表面湿润,较黏并呈半透明状,有凸面隆。透射电镜下,菌体呈长杆状,大小0.7~1.1 μm×2.0~4.0 μm,鞭毛单端丛生(图1),能运动。革兰氏染色呈阴性,无芽孢和荚膜。
图1
2.2 菌株HZ-2的生理生化特征
表1 产嗜铁素菌株HZ-2的生理生化特征
| 测定项目 | 结果 | 测定项目 | 结果 |
|---|---|---|---|
| 接触酶 | + | MR实验 | + |
| 氧化酶 | + | 葡萄糖利用 | + |
| 反硝化实验 | - | D-半乳糖利用 | + |
| 明胶液化 | - | 阿拉伯糖利用 | + |
| 柠檬酸盐利用 | - | 甘露糖利用 | + |
| 精氨酸双水解 | + | D-木糖利用 | + |
| V-P实验 | - | D-果糖利用 | + |
| 淀粉水解 | + | 肌醇利用 | + |
| 最高耐盐(7%) | + | 山梨醇利用 | + |
注:+表示反应呈阳性,-表示反应呈阴性。最高生长温度40 ℃生长,42 ℃不生长,4 ℃生长不定。
2.3 菌株HZ-2的脂肪酸分析
依照MIDI系统鉴定标准操作手册,当相似系数SI值大于0.5,而且第一匹配值和第二匹配值相差大于0.1时,认为鉴定成功,所参试的菌株可以鉴定为第一匹配值所呼应的菌名。本试验的结果表明第一选择SI值0.761,而且第一匹配值和第二匹配值相差大于0.1。因此,可以将菌株HZ-2鉴定为表2中第一匹配值对应的菌名恶臭假单胞菌(Pseudomonas putida)。
表2 菌株HZ-2的脂肪酸鉴定结果
| Library | Sim Index | Entry Name |
|---|---|---|
| TSBA6 6.10 | 0.761 | Pseudomonas-putida-biotype B/vancouverensis |
| 0.631 | Pseudomonas-fluorescens-biotype G/taetrolens | |
| 0.577 | Pseudomonas-putida-biotype A | |
| 0.510 | Pseudomonas-savastanoi-fraxinus | |
| 0.483 | Pseudomonas-fluorescens-biotype C/P. mandelii | |
| 0.457 | Pseudomonas-fluorescens-biotype B |
2.4 菌株HZ-2的16S rDNA序列分析
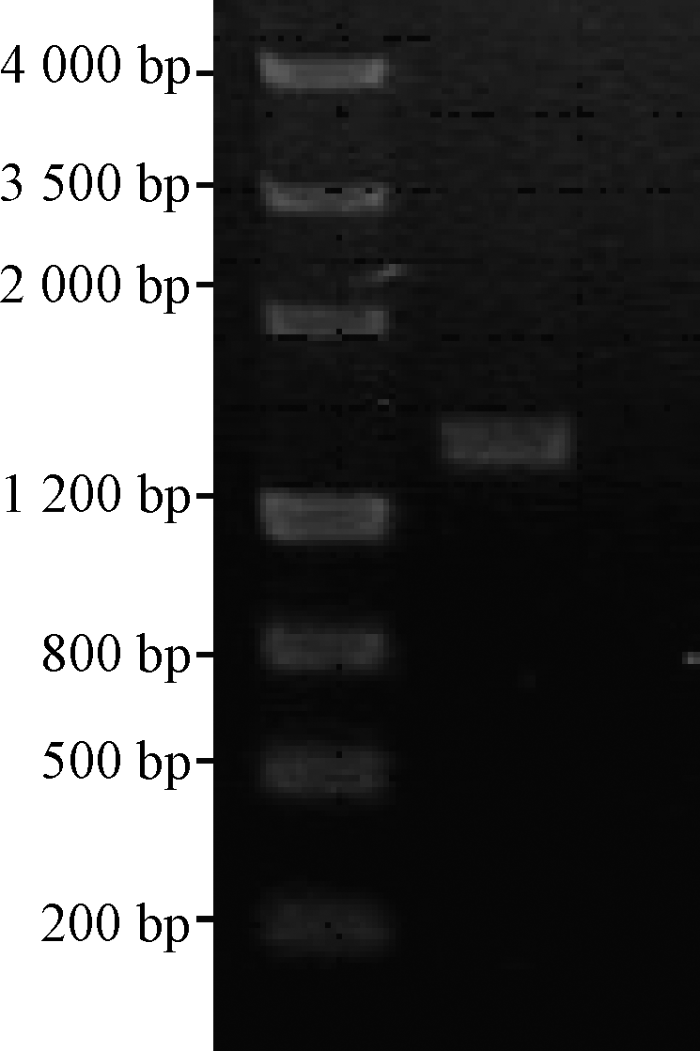
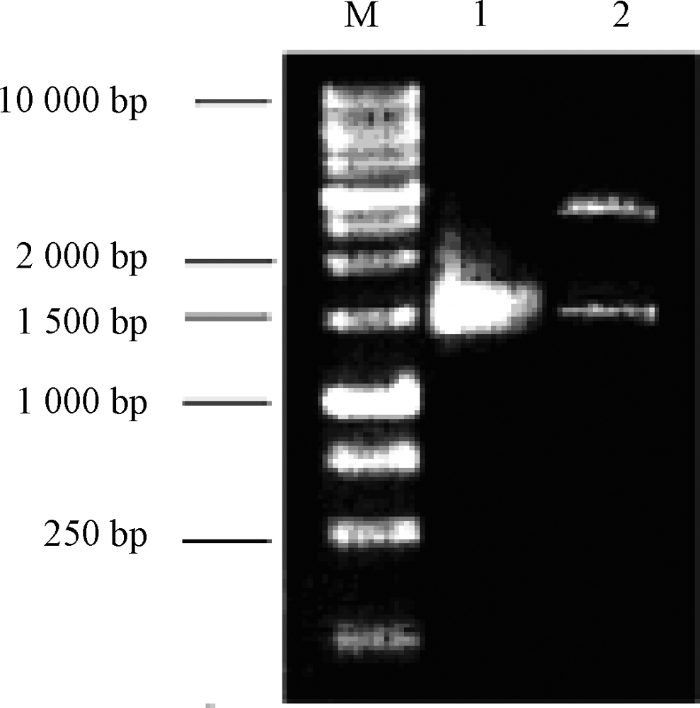
以菌株HZ-2的基因组DNA为模板,PCR扩增后电泳检测得到一条大小约1.5 kb的特异性条带(图2),与已报道的序列长度相吻合[20,23-24]。重组质粒经限制性内切酶EcolⅠ和PstⅠ双酶切后电泳检测,同样得到大小约为1.5 kb 左右的片段(图3),这表明菌株HZ-2的16S rDNA片段已经成功克隆到pGEM-T Vector中。测定克隆质粒的16S rDNA基因全序列,用软件录入,转化为GenBank信息库形式。BLAST同源序列检索结果表明,菌株HZ-2与GenBank收录的恶臭假单胞菌(Pseudomonas putida)基因序列相似性最高,达到99%。结合本试验中结果可将菌株HZ-2鉴定为恶臭假单胞菌(Pseudomonas putida)。
图2
图3
2.5 嗜铁素的定性检测
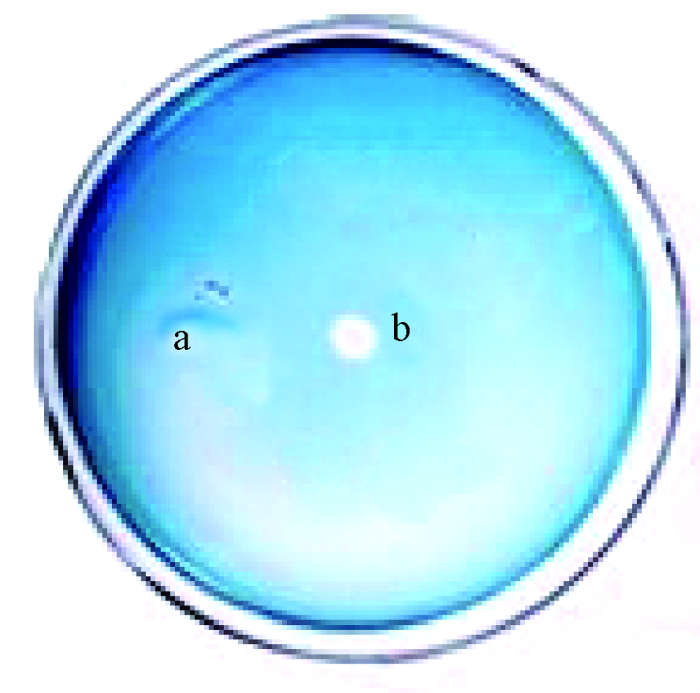
挑取单个菌落在通用CAS平板上点种,以大肠埃希菌HB101作为对照菌株,如图4所示,由于大肠埃希菌HB101菌株的嗜铁素合成基因(entE)没有缺失,但是培养10 h内,菌株HZ-2菌落b处产生了明显的橙红色晕圈,随着培养时间的延长,橙红色晕圈逐渐变大,经多次传代,其嗜铁素产生能力没有变化。而大肠埃希菌HB101菌落a处没有晕圈产生,证明了菌株HZ-2能够产生嗜铁素,而且产嗜铁素能力很强并且很快。
图4
2.6 嗜铁素的定量检测
菌株HZ-2产嗜铁素的A值为0.067,Ar值为1.353,A/Ar值为0.049。参照嗜铁素合成能力标准[25]可以断定,HZ-2产嗜铁素的能力属于极强范围。
3 讨论
近年来微生物鉴定自动化系统的开发和运用以其快速准确的优点得到了广泛关注,本文运用Sherlock MIS微生物鉴定系统,对产嗜铁素菌株进行了鉴定,与常规形态特征观察、生理生化指标测定结果以及16S rDNA基因全序列分析结果相一致,表明脂肪酸(FAME)鉴定法是一种有效的鉴定手段。
嗜铁素的定量检测目前一般采用CAS法,该方法以A/Ar的比值大小相对定量微生物分泌嗜铁素的能力。为确保结果的准确,实验需要注意2个环节:首先是要把控反应达到平衡的时间点,而一些研究报告[26]忽略了这点,其次是测试中菌悬液的处理问题。本实验待反应显色稳定后,并采用高速冷冻离心技术对菌悬液进行了处理,这样保证了结果的精确性。
参考文献
Current review siderophores in microbial interactions on plant surfaces
[J].
Iron withholding by plant polyphenols and resistance to pathogens and rots
[J].
Iron-responsive gene regulation in a Campylobacter jejuni fur mutant
[J].
Siderophores: structure and function of microbial iron transport compounds
[J].
The alternative nitrogenase of Azotobacter chroococcum is a vanadium enzyme
[J].
The response of Pseudomonas aeruginosa to iron: genetics, biochemistry and virulence
[J].
Microbial siderophores and their potential applications: a review
[J].
Ferric uptake regulation protein Acts as a repressor, employing iron(II) as a cofactor to bind the operator of an iron transport operon in Escherichia coli
[J].
Iron transport and storage
[J].
Bergey's Manual of Determinative Bacteriology
[M].
Laboratory guide for identification of plant pathogenic bacter
[M].
Design and evaluation of PCR primers to amplify bacterial 16S ribosomal DNA fragments used for community fingerprinting
[J].
Production of siderophores by the bacterium Kosakonia radicincitans and its application to control of phytopathogenic fungi
[J].
Growth of bacteria in an iron-free medium
[J].
Tn5 mutagenesis of Chinese Rhizobium fredii for siderophore overproduction
[J].